Роль химии в живописи и реставрации. Картина химия
Роль химии в живописи и реставрации
Живопись, как вид искусства существует с V века до н. э. Из всей живой природы только человек способен к творчеству. Произведения живописи отражают и оценивают эпоху, в которую были созданы. Поэтому человечество бережно хранит произведения искусства. В настоящее время проблема сохранения живописи стала актуальной, так как человек осознал, насколько хрупки творения великих мастеров. Но именно в наш «информационный» век стало возможным понять, как же именно сохранить произведения искусства. Этому способствуют науки: физика, математика и, в большей степени, химия.
Слово «реставрация» в переводе с греческого языка означает «восстановление». Во времена Петра I многие художники брали на себя обязанности «поновителя» - так тогда называли реставраторов. «Поновители» чаще всего дописывали недостающие фрагменты полотен или подновляли красочный слой, повторно покрывая его краской. Естественно, это производилось не без ущерба для картины.
В наше время процесс реставрации более совершенен. Каждая картина перед реставрацией подвергается химическому обследованию. Реставраторы прибегают к использованию только тех веществ, которые по своему составу повторяют или близки к оригиналу. Природных красок не так много, однако на картине очень трудно определить, какая именно краска использована. Здесь и приходят на помощь химики. После того как сделаны предварительные испытания, производят обнаружение катионов и анионов. В аналитической химии анализ смеси ионов проводят систематическим или дробным методом. В этом случае применяют характерные реакции, обладающие достаточной чувствительностью и избирательностью действия, позволяющие обнаружить искомый ион в присутствии всех остальных ионов.
Исследование белых пигментов.
Белые пигменты входят в состав красок:
Известковые белила (СаСО3). Растворяются в кислотах с выделением углекислого газа (СО2). В раствор переходят ионы Са2+.
Са СО3 + 2HCl → CaCl2 + CO2 + h3O
Открываемый ион Са2+ (II аналитическая группа катионов). Обнаружение Са2+. На предметное стекло помещают каплю исследуемого раствора и отдельно – каплю 2н раствора h3SO4. Капли соединяют при помощи капли воды. Через несколько минут в водной зоне выпадают кристаллы гипса, имеющие вид игл, розеток, пластинок.
Баритовые белила (ВаSO4). Нерастворимы в кислотах. Для перевода в раствор частицу пигмента сплавляют в тигле с содой (NaHCO3). В раствор переходят ионы Ba 2+. Открываемый ион Ba2+ (II аналитическая группа катионов). Обнаружение Ba2+. Каплю солянокислого раствора выпаривают досуха, смачивают каплей уксусной кислоты, рядом помещают каплю раствора бихромата калия, капли соединяют стеклянной палочкой. Выпадает осадок хромата бария BaCrO4 светло-желтого цвета.
2BaCl2 + K2Cr2O7 + h3O = 2BaCrO4 + 2KCl + 2HCl
2 Ba2+ + Cr2O72- + h3O = 2BaCrO4↓ + 2H+
Цинковые белила (ZnO). Растворяются в азотной кислоте, без выделения газа. В раствор переходят ионы Zn2+.
Zn О + 2HNO3→Zn( NO3)2 + h3O
Открываемый ион: Zn2+ (III аналитическая группа катионов). Обнаружение Zn2+. К капле азотнокислого раствора прибавляют 0,1%-ную каплю раствора сульфата меди и каплю тетрароданомеркуриата аммония.
Zn2+ + Cu 2+ + 2[Hg(SCN)4]2-= Zn [Hg(SCN)4]·Cu[Hg(SCN)4]
Свинцовые белила(PbOH)2CO3. Растворяются в кислотах с выделением углекислого газа (СО2). В раствор переходит ионы Рd2+
(РbОН)2 СО3 + 4HCl → 2PbСl 2 + CO2 + 3h3O
Открываемый ион: Pb2+ ( IV аналитическая группа катионов). Обнаружение Pb2+. C йодидом калия KI:
Pb2+ + 2KI = PbI2↓ + 2K+
На предметном стекле к капле исследуемого раствора прибавляют каплю 2 н. раствора Ch4COOH и каплю 0,1 н. раствора KI. В присутствии Pb2+ выпадают желтые кристаллы в форме треугольников или шестиугольников.
Исследование синих пигментов
Синие пигменты входят в состав красок:
Азурит(CuOH)2CO3, Растворяется в кислотах с выделением углекислого газа CO2. Открываемый ион- Cu2+(катион IV аналитической группы) переходит в раствор. Обнаружение Cu2+. К капле слабоуксуснокислого раствора добавляют каплю раствора тетрароданомеркуриата аммония. Образуются желтые кристаллы Cu[Hg(CNS)4]
Cu2+ + [Hg(SCN)4]2- = Сu[Hg(SCN)4] ↓
Берлинская лазурь (Fe4[Fe(CN)6]3). Нерастворимое в кислотах соединение, разлагается щелочами, образуя гидроксид Fe (III) и ферроцианид калия K4[Fe(CN)6]. 4Fe3+ + 3K4SCN = Fe(SCN)3↓ + 12K+
Открываемый ион-Fe3+(катион III аналитической группы) переходит в раствор. Обнаружение Fe3+: в пробирку помещают 1-2 капли исследуемого раствора, 1-2 капли 2 н. раствора HCl и 3-4 капли роданида калия. Образуется роданид железа кроваво-красного цвета Fe(SCN)3.
K4[Fe(CN)6] + 12КОН = 4Fe(OH)3 + 3K4[Fe(CN)6]
K4[Fe(CN)6] + 12OH- = 4Fe(OH)3+ 3[Fe(CN)6]4-
Смальта (калиевое силикатное стекло, окрашенное кобальтом). Пигмент переводят в раствор, сплавляя с фтористым натрием (NaF). Полученную массу растворяют в воде. Открываемый ион-Co2+(катион IV аналитической группы) переходит в раствор. Обнаружение Co2+. Каплю нейтрального или уксуснокислого раствора упаривают на предметном стекле. К сухому остатку добавляют каплю тетрароданомеркуриата аммония. Образуются синие кристаллы Co[Hg(CNS)4] в виде призм, пирамид, треугольников.
Co2+ + [Hg(SCN)4]2- = Co [Hg(SCN)4] ↓
Александрийская лазурь (медное стекло), Пигмент переводят в раствор, сплавляя с фтористым натрием (NaF). Полученную массу растворяют в воде. Открываемый ион- Cu2+(катион IV аналитической группы) переходит в раствор Обнаружение Cu2+. К капле слабоуксуснокислогo раствора добавляют каплю раствора тетрароданомеркуриата аммония. Образуются желтые кристаллы Cu[Hg(CNS)4]
Cu2+ + [Hg(SCN)4]2- = Сu[Hg(SCN)4] ↓
Натуральный и искусственный ультрамарин (Na8-10 Al6 Si6O24 S24) (лазурит). Разлагается в кислотах с выделением сероводорода h3S. Открываемый ион- S2- (анион I аналитической группы). Обнаружение S2-: полоску фильтровальной бумаги смачивают раствором ацетата свинца (Сh4COO)2Pb. К 2-3 каплям анализируемого раствора добавляют 3-4 мл 2 н. раствора HCl. Пробирку накрывают полоской фильтровальной бумаги и слегка нагревают. Происходит почернение бумажки, пропитанной ацетатом.
Исследование красных пигментов
Киноварь(Природный минерал и искусственно получаемый сульфид ртути HgS)
Растворяется в царской водке при нагревании. Открываемый ион- Hg 2+(IV аналитическая группа катионов) переходит в раствор. Обнаружение Hg2+: к капле раствора, содержащего ртуть, прибавляют каплю смеси концентрированных растворов роданида аммония Nh5CNS и нитрата кобальта Co(NO3)2. Образуются темно-синие кристаллы Co[ Hg(CNS)4] в виде игл, призм.
Реальгар (природный минерал состава As2S). Растворяется в концентрированной HNO3. Открываемый ион- As5+ переходит в раствор. Обнаружение As5+: к капле раствора, содержащего мышьяк, добавляют каплю азотной кислоты и крупинку молибдата аммония (Nh5)2Mo4. При этом образуется желтый кристаллический осадок (Nh5)3AsO4·12MoO3 в виде мелких кубов, октаэдров.
HNO3. As5+ переходит в раствор. Сурьмяная красная( Sb2S3 (искусственный)). Для перевода в раствор растворяют в концентрированной HCl. Открываемый ион-Sb3+ Обнаружение Sb3: в каплю исследуемого раствора вводят кристаллик йодистого калия KI и через некоторое время кристаллик йодистого хлористого цезия CsCl. В присутствии сурьмы образуются оранжевые кристаллы Cs2SbI.
Красный кадмий (сульфид и селенид кадмия CdS·CdSe). Концентрированные кислоты растворяют пигмент с выделением сероводорода и селеноводорода.
Открываемые ионы: a) Cd2+. Обнаружение Cd2+:в каплю нейтрального раствора помещают крупинку щавелевой кислоты или оксалата аммония. Концентрированные кислоты растворяют пигмент с выделением сероводорода и селеноводорода. Образуется бесцветный кристаллический осадок оксалата кадмия CdC2O4·3h3O в виде призм и ромбов б) Se2-. Обнаружение Se2-:на фильтровальную бумагу помещают немого порошка тиомочевины, затем – каплю исследуемого раствора. Образуется кроваво-красный селен Se.
Красный хром (основной хромат свинца PbCrO4·PbO). Растворяется в неорганических кислотах. Открываемые ионы: Pb2+ (IV анал. группа), бихромат CrO42(II группа анионов) переходит в раствор.
а) Обнаружение Pb2+: На предметном стекле к капле исследуемого раствора прибавляют каплю 2 н. раствора Ch4COOH и каплю 0,1 н. раствора KI. В присутствии Pb2+ выпадают ярко-желтые кристаллы йодида свинца PbI2, Которые растворяются в воде. При охлаждении раствора вновь выпадает осадок PbI2 в виде золотисто-желтых пластинчатых кристаллов.
б) Обнаружение Cr2O72-. Частицу пигмента растворяют в 3%- ной уксусной кислоте. В полученный раствор вводят кристалл нитрата серебра AgNO3. Реакции мешает большое количество хлоридов. Образуются красно-оранжевые кристаллы бихромата серебра Ag2Cr2O7 исследование зеленых пигментов
Ярь-медянка (собирательный термин для ацетатов меди различного химического состава):
2Cu(Ch4COO)2∙Cu(OH)2∙5h3O
Cu (Ch4COO)2∙ Cu(OH)2∙5h3O
Cu (Ch4COO)2∙2Cu(OH)2
Cu (Ch4COO)2∙h3O
Хорошо растворяется в кислотах. Щелочи взаимодействуют с ярью-медянкой, образуя гидроксид меди синего цвета. Все медные зеленые пигменты при нагревании до высоких температур разлагаются до оксида меди (II) CuO черного цвета.
Открываемые ионы:
А) Cu2+ (катион IV аналитической группы). Обнаружение: к капле исследуемого раствора добавляют каплю раствора тетрароданомеркуриата аммония. Образуются желтые кристаллы Cu[Hg(CNS)4]
Cu2+ + [Hg(SCN)4] 2- = Cu[Hg(SCN)4]↓
Б) Ch4COO-. Обнаружение: частицу пигменты смешивают со смесью равных частей оксида кальция и углекислого кальция, помещают в стеклянную трубку, запаянную с одного конца. Открытый конец трубки накрывают ф/бумагой, пропитанной раствором ортонитробензальдегида, и постепенно нагревают трубку. Фильтровальная бумага становится синей или сине-зеленой.
Малахит природный натуральный (СuCO3∙Cu(OH)2)
Взаимодействует с кислотами с выделением углекислого газа, что резко отличает его от всех медных зеленых пигментов.
Открываемый ион:Cu2+(катион IV аналитической группы). Обнаружение: к капле исследуемого раствора добавляют каплю раствора тетрароданомеркуриата аммония. Образуются желтые кристаллы Cu[Hg(CNS)4].
Cu2+ + [Hg(SCN)4] 2- = Cu[Hg(SCN)4]↓
Зеленая шееле (осноной метаарсенит меди Cu(AsO2)∙nCu(OH)2∙mh3O)Легко растворяется в кислотах и щелочах.
А) Cu2+ (катион IV аналитической группы). Обнаружение: к капле исследуемого раствора добавляют каплю раствора тетрароданомеркуриата аммония. Образуются желтые кристаллы Cu[Hg(CNS)4]
Cu2+ + [Hg(SCN)4] 2- = Cu[Hg(SCN)4]↓
Б) As (V). Обнаружение: к исследуемому раствору добавляют каплю азотной кислоты и крупинку молибдата аммония. Образуется желтый кристаллический осадок (Nh5)3AsO4∙12MoO3 в виде мелких кубов и октаэдров.
Швейнфутская зелень (арсенит-ацетат меди, Cu(Ch4COO)2∙3 Cu(AsO2)2)
Легко растворяется в кислотах и щелочах.
Открываемые ионы:
А) Cu2+ (катион IV аналитической группы). Обнаружение: к капле исследуемого раствора добавляют каплю раствора тетрароданомеркуриата аммония. Образуются желтые кристаллы Cu[Hg(CNS)4].
Cu2+ + [Hg(SCN)4] 2- = Cu[Hg(SCN)4]↓
Б)As (V). Обнаружение: частицу пигменты смешивают со смесью равных частей оксида кальция и углекислого кальция, помещают в стеклянную трубку, запаянную с одного конца. Открытый конец трубки накрывают ф/бумагой, пропитанной раствором ортонитробензальдегида, и постепенно нагревают трубку. Образуется желтый кристаллический осадок.
В) (Ch4COO)2-. К исследуемому раствору добавляют каплю азотной кислоты и крупинку молибдата аммония. Фильтровальная бумага становится синей или сине-зеленой.
Исследование черных пигментов
Помимо ламповой копоти и древесного угля в качестве черных пигментов использовались пережженная виноградная лоза и персиковые косточки, а также слоновая кость. Черные пигменты, полученные при сжигании растений, практически полностью состоят из углерода, тогда как пигменты, полученный из животных костей, содержат лишь около 10 % углерода; основная же их часть – фосфат магния Mg3(PO4)2 и карбонат кальция СаСo3. Поэтому, если после прокаливания исследуемой пробы остается минеральный остаток, необходимо его проанализировать на присутствие ионов Са2+, PO43- , Mg2+.
Обнаружение Mg2+. На предметное стекло помещают каплю исследуемого раствора, обрабатывают парами аммиака и вносят кристаллик Na2HPO4. Выпадают кристаллы белого цвета MgNh5PO4
В виде звездочек и пирамид. Реакции мешают ионы Са2+, которые удаляют с помощью раствора углекислого аммония (Nh5)2СО3 в присутствии оксалата аммония.
Обнаружение PO43-. Остаток, полученный после прокаливания , растворяют в разбавленной азотной кислоте (Cl- должен отсутствовать). К капле полученного раствора добавляют каплю реактива (1 г. (Nh5)2MoO4 растворяют в 12 мл HNO3 и слегка нагревают. Выпадет желтый осадок аммонийной соли фосфоромолибденовой кислоты ((Nh5)3h5[P(Mo2O7)6]. Осадок растворяется в избытке фосфата, поэтому реактив необходимо прибавлять в большом избытке. Чувствительность реакции повышается при добавлении твердого нитрата аммония Nh5NO3.
Na2HPO4 + 12(Nh5)2MoO4 + 23 HNO3 =
= (Nh5)3h5[P(Mo2O7)6]↓ + 2NaNO3 + 21Nh5NO3 + 10h3O
HPO42-+ 3H+4 + 12Mo42- + 23H+ = (Nh5)3h5[P(Mo2O7)6] ↓ + 10h3O
Металлические пигменты
Металлические пигменты – тонкодисперсные порошки, либо тончайшие листки – по составу представляют собой металлы или их сплавы. Среди минеральных пигментов они выделяются металлическим блеском. Для исследования состава металлических пигментов последовательно проводят операции растворения микропроб в различных кислотах, наблюдение цветовых изменений при нагревании до 1000оС и обнаружении с помощью специфических реакций катионов металлов.
Пигменты из золота. Порошковое либо листовое золото легко отличить от других золотистых пигментов – меди и ее сплавов: золото не растворяется ни в одной кислоте, за исключением царской водки, и не изменяется при прокаливании до 1000 оС.
Обнаружение Au(III). Частицу пигмента дважды обрабатывают царской водкой, выпаривают досуха. К сухому остатку добавляют каплю 2 н соляной кислоты. На фильтровальную бумагу наносят каплю анализируемого раствора и каплю бензидина. Реакции мешают большие количества тяжелых металлов, а также окистители, взаимодействующие с бензидином.
Пигменты из меди и ее сплавов. При прокаливании эти пигменты чернеют. Они хорошо растворяются в азотной кислоте при нагревании.
Пигменты из серебра. Серебро, также, как и золото, используется в виде порошка или тонких листов. Отличительная черта серебряного пигмента (в старении с другими металлическими серебристыми пигментами) – наличие темно-коричневой, практически черной пленки сульфида серебра Ag2S, образующейся в местах трещин и утрат покровного лака в результате воздействия сероводорода атмосферы.
Заключение.
В живописи часто используются одинаковые по цвету, но отличные по составу и кристаллической структуре пигменты. Отличить такие пигменты друг от друга помогает лаборатория микрохимического анализа. Аналитическая химия «спасла» многие работы, вовремя подсказав, какой материал нужно использовать. Новейшие технологии (атомарный кислород, нано-технологии) способствуют дальнейшему развитию реставрации, ее выходу на совершенно иной технологический уровень. Таким образом, химия способствует сохранению художественных произведений.
В целом, искусство очень тесно связано с химией. Материалы, использующиеся художниками нелишне рассматривать и с научной точки зрения, так как научное осмысление творчества приводит к достижению новых результатов. Химия раскрывает «тайну» картин и их разрушения со временем. Химия же помогает создавать картины и возвращать их к жизни.
И юным химикам, и химикам ос стажем будет интересно ознакомиться с исторической и научной точкой зрения на химию в искусстве. А художникам узнать, что же представляет из себя искусство на молекулярном уровне. В реставрации наука и искусство как никогда близки.
www.hintfox.com
| Обратная связь | (структурные уровни организации материи с точки зрения химии).
Химия – одна из отраслей естествознания, предметом изучения которой являются химические элементы (атомы), образуемые ими простые и сложные вещества (молекулы), их превращения и законы, которым подчиняются эти превращения. По определению Д.И. Менделеева (1871), "химию в современном ее состоянии можно назвать учением об элементах". Происхождение слова "химия" выяснено не окончательно. Многие исследователи полагают, что оно происходит от старинного наименования Египта – Хемия (греч. Chemía, встречается у Плутарха), которое производится от "хем" или "хаме" – черный и означает "наука черной земли" (Египта), "египетская наука". Современная химия тесно связана как с другими науками, так и со всеми отраслями народного хозяйства. Качественная особенность химической формы движения материи и ее переходов в другие формы движения обусловливает разносторонность химической науки и ее связей с областями знания, изучающими и более низшие, и более высшие формы движения. Познание химической формы движения материи обогащает общее учение о развитии природы, эволюции вещества во Вселенной, содействует становлению целостной материалистической картины мира. Соприкосновение химии с другими науками порождает специфические области взаимного их проникновения. Так, области перехода между химией и физикой представлены физической химией и химической физикой. Между химией и биологией, химией и геологией возникли особые пограничные области - геохимия, биохимия, биогеохимия, молекулярная биология. Важнейшие законы химии формулируются на математическом языке и теоретическая химия также не может развиваться без математики. Химия оказывала и оказывает влияние на развитие философии и сама испытывала и испытывает ее влияние. Исторически сложились два основных раздела химии: неорганическая химия, изучающая в первую очередь химические элементы и образуемые ими простые и сложные вещества (кроме соединений углерода), и органическая химия, предметом изучения которой являются соединения углерода с другими элементами (органические вещества). До конца 18 в. термины "неорганическая химия" и "органическая химия" указывали лишь на то, из какого "царства" природы (минерального, растительного или животного) получались те или иные соединения. Начиная с 19 в. эти термины стали указывать на присутствие или отсутствие углерода в данном веществе. Затем они приобрели новое, более широкое значение. Неорганическая химия соприкасается прежде всего с геохимией и далее с минералогией и геологией, т.е. с науками о неорганической природе. Органическая химия представляет отрасль химии, которая изучает разнообразные соединения углерода вплоть до сложнейших биополимерных веществ; через органическую и биоорганическую химию Химия граничит с биохимией и далее с биологией, т.е. с совокупностью наук о живой природе. На стыке между неорганической и органической химией находится область элементоорганических соединений. В химии постепенно сформировались представления о структурных уровнях организации вещества. Усложнение вещества, начиная от низшего, атомарного, проходит ступени молекулярных, макромолекулярных, или высокомолекулярных, соединений (полимер), затем межмолекулярных (комплекс, клатрат, катенан), наконец, многообразных макроструктур (кристалл, мицелла) вплоть до неопределенных нестехиометрических образований. Постепенно сложились и обособились соответствующие дисциплины: химия комплексных соединений, полимеров, кристаллохимия, учения о дисперсных системах и поверхностных явлениях, сплавах и др. Изучение химических объектов и явлений физическими методами, установление закономерностей химических превращений, исходя из общих принципов физики, лежит в основе физической химии. К этой области химии относится ряд в значительной мере самостоятельных дисциплин: термодинамика химическая, кинетика химическая, электрохимия, коллоидная химия, квантовая химия и учение о строении и свойствах молекул, ионов, радикалов, радиационная химия, фотохимия, учения о катализе, химических равновесиях, растворах и др. Самостоятельный характер приобрела аналитическая химия, методы которой широко применяются во всех областях химии и химической промышленности. В областях практического приложения химии возникли такие науки и научные дисциплины, как химическая технология с множеством ее отраслей, металлургия, агрохимия, медицинская химия, судебная химия и др. Внешний мир, существующий независимо от человека и его сознания, представляет собой различные виды движения материи. Материя существует в вечном движении, мерой которого выступает энергия. Наиболее изучены такие формы существования материи как вещество и поле. В меньшей степени наука проникла в сущность вакуума и информации как возможных форм существования материальных объектов.
Под веществом понимают устойчивую совокупность частиц (атомов, молекул и др.), обладающих массой покоя. Поле рассматривается как материальная среда, обеспечивающая взаимодействие частиц. Современная наука считает, что поле представляет собой поток квантов, не обладающих массой покоя. Окружающие человека материальные тела состоят из различных веществ. При этом телами называют объекты реального мира, обладающие массой покоя и занимающие определенный объем пространства. Каждое тело имеет свои физические параметры и свойства. А вещества, из которых они состоят, обладают химическими и физическими свойствами. В качестве физических свойств можно назвать агрегатные состояния вещества, плотность, растворимость, температура, цвет, вкус, запах и др. Различают твердое, жидкое, газообразное и плазменное агрегатные состояния вещества. В нормальных условиях (температура 20 градусов Цельсия, давление 1 атмосфера) различные вещества находятся в разных агрегатных состояниях. Например: сахароза, хлорид натрия (соль), сера – это твердые тела; вода, бензол, серная кислота – жидкости; кислород, диоксид углерода, метан – газы. Главной задачей химии как науки является выявление и описание таких свойств вещества, которые позволяют превращать одни вещества в другие на основе химических реакций. Химические превращения – это особая форма движения материи, которая обусловлена взаимодействием атомов, приводящим к образованию молекул, ассоциантов и агрегатов. С точки зрения химической организации атом является исходным уровнем в общей структуре материи. Химия, таким образом, изучает особую «химическую» форму движения материи, характерной особенностью которой является качественное превращение вещества. Химия – это наука, изучающая превращение одних веществ в другие, сопровождающееся изменением их состава и структуры, а также исследует взаимные переходы между этими процессами. Термин «естествознание» означает знание о природе или природоведение. Начало изучению природы положила натурфилософия («природоведение» в переводе с немецкого «naturphilosophie»; а в переводе с латинского – «natura» – природа, «Sophia» – мудрость). В ходе развития каждой науки, в том числе и химии, развивался математический аппарат, понятийный аппарат теорий, совершенствовалась экспериментальная база и техника эксперимента. Как результат возникла полная дифференциация в предметах исследования различных естественных наук. Химия в основном исследует атомный и молекулярный уровень организации материи, что представлено на рис. 8.1.
Рис. 8.1.
Рис. 8.1. Уровни материи, изучаемые химической наукой Основные понятия и законы химии
В основе современного естествознания лежит принцип сохранения материи, движения и энергии. Сформулированный М.В. Ломоносовым в 1748 г. Этот принцип прочно вошел в химическую науку. В 1756 г. М.В. ломоносов, изучая химические процессы, обнаружил постоянство общей массы веществ, участвующих в химической реакции. Это открытие стало важнейшим законом химии – законом сохранения и взаимосвязи массы и энергии. В современной трактовке он формулируется следующим образом: масса веществ, вступивших в химическую реакцию, равна массе веществ, образовавшихся в результате реакции. В 1774 г. Знаменитый французский химик А. Лавуазье дополнил закон сохранения массы представлениями о неизменности масс каждого из веществ, участвующих в реакции. В 1760 г. М.В. Ломоносов сформулировал закон сохранения энергии: энергия не возникает из ничего и не исчезает бесследно, она превращается из одного вида в другой. Немецкий ученый Р. Майер в 1842 г. Экспериментально подтвердил данный закон. А английский ученый Джоуль установил эквивалентность различных видов энергии и работы (1кал= 4,2 Дж). Для химических реакций этот закон формулируется следующим образом: энергия системы, включающей вещества, вступившие в реакцию, равна энергии системы, включающей вещества, образовавшиеся в результате реакции. Закон постоянства состава был открыт французским ученым Ж. Прустом (1801г.): всякое химически чистое индивидуальное вещество имеет всегда один и тот же количественный состав независимо от способа его получения. Другими словами, как бы не получали воду –при сгорании водорода или при разложении гидроксида кальция (Ca (OH)2 ) отношение масс водорода и кислорода в ней равно 1:8. В 1803г. Дж. Дальтон (английский физик и химик) открыл закон кратных отношений, согласно которому, если два элемента образуют между собой несколько соединений, то массы одного из элементов, приходящиеся на одну и ту же массу другого, относятся между собой как небольшие целые числа. Этот закон является подтверждением атомистических представлений о структуре материи. Если элементы соединяются в кратных отношениях, то химические соединения различаются на целые атомы, которые представляют собой наименьшее количество элемента, вступившего в соединение. Важнейшим открытием химии XIX столетия является закон Авогадро. В результате количественных исследований реакций между газами французский физик Ж.Л. Гей-Люссак установил, что объемы реагирующих газов относятся между собой и к объемам образующихся газообразных продуктов, как небольшие целые числа. Объяснение этому факту и дает закон Авогадро (открытый итальянским химиком А. Авогадро в 1811г.): в равных объемах любых газов, взятых при одинаковой температуре и давлении, содержится одинаковое число молекул. Закон эквивалентов часто применяется в химических расчетах. Из закона постоянства состава следует, что взаимодействие элементов друг с другом совершается в строго определенных (эквивалентных) соотношениях. Поэтому термин эквивалент утвердился в химической науке в качестве основного. Эквивалентом элемента называют такое его количество, которое соединяется с одним молем водорода или замещает тоже количество атомов водорода в химических реакциях. Масса одного эквивалента химического элемента называется его эквивалентной массой. Представления об эквивалентах и эквивалентных массах применимы и к сложным веществам. Эквивалентом сложного вещества называется такое его количество, которое взаимодействует без остатка с одним эквивалентом водорода или с одним эквивалентом любого другого вещества. Формулировка закона эквивалентов была дана Рихтером в конце XVIII века: все вещества реагируют друг с другом в количествах, пропорциональных их эквивалентам. Другая формулировка этого закона гласит: массы (объемы) реагирующих друг с другом веществ пропорциональны их эквивалентнвм массам (объемам). Математическая запись этого закона имеет вид: m1: m2 = Э 1: Э 2, где m 1 и m 2 – массы взаимодействующих веществ, Э 1 и Э 2 – эквивалентные массы этих веществ, выраженные в кг/моль. Важную роль играет периодический закон Д.И. Менделеева, современная трактовка которого гласит, что порядок расположения и химические свойства элементов определяются зарядом ядра.
| |
pdnr.ru
Химия в живописи — OrenWiki
Название проекта
Химия в живописи
Авторы и участники проекта
Учащиеся 9 класса (слушатели элективного курса "Мир искусства глазами химика"
Тема исследования группы
Вещества, используемые художниками для написания картин
Проблемные вопросы
1.Какие жанры изобразительного искусства существуют?
2.Из чего состоят краски? Какие бывают краски?
3.Можно ли получить краски в лаборатории?
4.Что такое пигменты? Что входит в их состав?
Результаты исследования
Жи́вопись — вид изобразительного искусства, связанный с передачей зрительных образов посредством нанесения красок на твёрдую или гибкую поверхность.
Существует два вида живописи: станковая и монументальная. К станковой живописи относят произведения, существующие независимо от места создания. В основном это картины, созданные на мольберте (то есть станке) художника. В станковой живописи преобладают работы выполненные масляными красками, но могут использоваться и другие красители (темпера, акриловые краски и т.д.). Картины пишутся в основном на холсте, натянутом на раму или наклеенном на картон, на картоне, в прошлом широко применялись деревянные доски, могут использоваться любые плоские материалы. Монументальная живопись выполняется непосредственно на стенах зданий и других сооружений. В прошлом преобладала живопись темперными красками по сырой штукатурке (фреска). Однако эта техника сложна, поэтому применяют и другие технологии, например масляные краски. Цветные изображения на бумаге (акварель, гуашь, пастель и др.) формально (например, по месту в коллекции) относят к графике, но эти произведения часто рассматриваюся и как живописные. Различают следующие жанры живописи: Анималистический, батальный,бытовой, исторический, мифологический, натюрморт, портрет и пейзаж. Подробнее
 Словарь терминов
Словарь терминов  Словарь терминов
Словарь терминов В живописи используют различные краски для рисования: акварельные, акриловые, гуашь, тушь, темперные, маясляные и другие. Все они состоят из пигментов, связующих материалов и пластификаторов. Подробнее Пигменты можно получить в лаборатории. Смотри инструкции Мы провели исследование некотрых пигментов на основе качественных реакций и создали таблицу- памятку для товарищей. Здесь Мы получили некоторые количества пигментов, на следующем занятии мы можем попробовать сделать из них акварельные и масляные краски, быть модет у нас получиться нарисовать ими картину!

Выводы
1.На сегодняшний день существует множество жанров изобразительного искусства: пейзаж, натюрморт и т.д.
2.Краски для рисования могут быть самыми различными, но все они содержат пигрменты и связующие вещества.
3.Даже в школьной лаборатории можно получить некоторые пигменты, из которых затем изготовить краски.
4.Пигменты- это минеральные или органические вещества, состав которых можно определить с помощью качественных реакций.
5.Химики действительно знают, как устроен мир - они помогают сделать его еще лучше!
Полезные ресурсы
Химические вещества и материалы в живописи
Исследование пигментов живописи при реставрации картин
Разработка элективного курса "Химия в изобразительном искусстве"
Ширшина Н.В. «Химия для гуманитариев», Волгоград, Учитель», 2004г
Титова И.М. «Вещества и материалы в руках художника», М. Мирос, 1994
http://youtu.be/vyscNaQ16Y8 - всемирная история живописи
http://youtu.be/W9p2hQyMLKA - картины И.К. Айвазовского
http://youtu.be/WwATriZfIcQ - памяти К.Брюллова
http://youtu.be/KNf3Czh2v1U
http://gallerix.ru/album/200-Russian - 200 русских живописцев
http://www.bibliotekar.ru/slovarZhivopis/index.htm - Живопись
http://www.bibliotekar.ru/muzeu.htm
http://youtu.be/AlVkbxANYSg - натюрморты
Другие документы
Рефлексия
www.orenwiki.ru
Реферат - Химия и искусство
Лицей №7 при ВГПУ
Химия и искусство.
Выполнила: Иванова Екатерина
11 «А» класс
Руководитель: Медведева И.А.
Воронеж
2005
Оглавление
Вступление 1
Химические вещества иматериалы в живописи 2
Методы исследованияпроизведений монументальной и станковой живописи 6
Изучение химическогосостава древней живописи в инфракрасных лучах 7
Металлы:
Металлы – материал длясоздания шедевров мирового искусства 8
О меди и бронзе 8
Позолота 11
Металлический блеск взеркалах 12
Железо и жесть 13
Чугун: и волшебство, ивдохновенье 14
Сталь: от оружия до…ювелирных изделий 16
Стекло:
Художественнаяценность и свойства стекла 17
Характеристика ихимический состав стекла 18
Способы производства иотделки стекла 19
Исторический обзорстеклопроизводства 20
Искусство керамики:
Обзорная характеристикасостава и свойств глинистых материалов. Каолин. 22
Виды керамики 23
Заключение 28
Вступление.
Я выбрала данную тему реферата, потому что мне захотелосьбольше узнать о тех произведениях искусства, которые нас окружают. Я имею ввиду картины, стеклянные, металлические, а также глиняные изделия. Оченьинтересно узнать, как зарождалось то или иное искусство в Мире.
В наше время существует великое множество украшений для быта,и все они имеют корни, уходящие глубоко в прошлое. С помощью усовершенствованиятехнологий мы наблюдаем различные изобретения человека в плане искусства, но ираньше они были не менее красивыми, хотя условия жизни были совершенно другимии значительно отличались от наших.
Многие из шедевров дошли до нас из глубины веков и радуют досих пор, а некоторые были утрачены из-за непрочности материалов. Чтобы добитьсянаилучшего качества своих красок и долговечности полотен, художнику зачастуюнужно быть не только изографом, но и химиком.
О свойствах и составе красок, о техниках и видах живописи,металлах, художественной ценности стекла, искусстве керамики и многом другомизложено в данном реферате.
Химия и искусство.
Химия и искусство имеют внутреннююобщность, которая коренится в их творческой природе.
Марселен Бертло
Химические вещества и материалы вживописи.
Как разнообразен и прекрасен мир искусства, особенноживопись! Какие уникальные картины и полотна созданы талантливыми художниками!Многие из шедевров дошли до нас из глубины веков и радуют до сих пор, анекоторые были утрачены из-за непрочности материалов. Чтобы добиться наилучшегокачества своих красок и долговечности полотен, художнику зачастую нужно быть нетолько изографом, но и химиком.
О свойствах и составе красок, о техниках и видах живописи ио многом другом вы узнаете из этого раздела.
Недостаточно знать различные виды красок, виды грунтов.Необходимо также уметь различать виды живописи и технику их использования. Одиниз самых удивительных видов живописи – энкаустика.Это живопись расплавленными твёрдыми красками, связующей основой которогоявляется воск. Существует древнегреческая легенда, рассказывающая о внезапномснятии осады г. Родоса в IIIвеке до нашей эры. Военные действия против родосцев возглавлял македонскийцарь, один из диадохов – преемников Александра Македонского, ДеметрийПолиоркет. Обстоятельства сложились так, что отряды Полиоркета должны были брать город с той стороны, где находилась мастерская знаменитого энкауста Протогена. Царь, боясь нанести ущербмастерской художника, приказал снять осаду… Эта удивительная легенда имеетпод собой реальную основу. В Древней Греции, особенно в период расцвета еёискусства ( VI-V вв. до н.э. ), энкаустическиекартины ценились необыкновенно высоко. Плиний Старший рассказывал, что лучшиепроизведения выдающегося художника того времени Зевксиса стоили так дорого, чтокупить их было невозможно, и автор просто дарил свои произведения.
К сожалению, до нашего времени не сохранилось ни однойстанковой энкаустической греческой картины. Вероятно, большая их часть былавывезена в Рим и погибла там во время пожаров (410 и 452 гг.). Сохранились лишьупоминания и описания таких картин. Например, можно привести высказывание обэнкаустике античного автора Флавия Филострата: «Искусство, основанное направде, вызывает капли росы на цветах, на них сидит даже пчела, и неизвестно,она ли обманута, или мы, в заблуждение введённые, считаем её живою».По-видимому, Плиний был отчасти прав, когда писал: «Мы будем говорить о том,что осталось от живописи, искусства некогда знаменитого». Впрочем, древниекартины, написанные энкаустическими красками, всё же дошли до нашего времени. Впервую очередь, это знаменитые фаюмские портреты из Египта, относящиеся к I-III столетиям. Особое впечатлениепроизводят яркость и свежесть красок, которыми они выполнены.
Прочность энкаустической живописи объясняется главнымобразом свойствами связующего – пчелиного воска. Этот материал способен в течениетысячелетий сохранять мягкость и эластичность, поскольку обладает свойством«дышать» вместе с деревянной основой картины, то есть сжиматься при понижениитемпературы и расширяться при её повышении, так же, как дерево. А посколькувоск водонепроницаем, то в результате температурных колебаний в нём невозникает трещин и разрывов.
Технология работы энкауста исключительно сложна. Как ужеговорилось, в этой технике применяются твёрдые краски, и для нанесения их наоснову (специально подготовленную доску) используют не кисть, а особыеинструменты, каутерии – бронзовые ложечки разных размеров, дно которых имееткилевидную форму. Хорошо нагретым наогне каутерием художник отделяет от большого куска маленькие кусочки краски ипомещает их в нужных местах создаваемого изображения. Киль ложечки служит дляразглаживания мазка. Эта кропотливая работа требует большого таланта и умения.
Когда роспись готова, для лучшего её закрепления всёполученное изображение прогревается с целью оплавления красок. Эта операция имеетпринципиальное значение. В составе энкаустических красок всегда содержитсянемного льняного масла. При оплавлении оно выступает на поверхность и после застывания образует тончайшуюстекловидную плёнку. Это и есть знаменитый энкаустический лак. Сложная висполнении энкаустическая техника позднее была вытеснена другими, болеепростыми – темперой и затем масляной живописью. Секрет приготовления энкаустикипостепенно был утрачен. Восстановить секрет забытой техники стремились многиеучёные и художники, в том числе и Леонардо да Винчи. Однако время еёвозрождения пришло позже: в 1935 году секреты древних были разгаданыпотомственным живописцем Василием Вениаминовичем Хвостенко. Успех пришёл врезультате выполнения множества опытов, в том числе химических.
Из курса истории все хорошо знают: стенная роспись, которойобычно украшались русские православные храмы, называется фреской. Первые киевские церкви – Десятинная, собор Святой Софии –были богато украшены мозаичными изображениями, выполненными из смальты. Однакосоздание мозаик – очень длительный и дорогой процесс, поэтому во второйполовине XI века онибыли вытеснены росписями, выполненными по сырой штукатурке. При созданиинаиболее древних фресок наряду с покупными минеральными красками русскиеизографы применяли цветные глины красных, жёлтых, коричневых, зелёных тонов.Эти глины тщательно растирали на воде. Попадавшие в них крохотные частичкикварца и слюды создавали особую фактуру живописи, слабое её мерцание.Современные её художники, копирующие старинные фрески, также используют вкачестве пигментов различные глины.
Однако фрески создавались не только на Руси. Это одна издревнейших живописных техник, которую использовали художники разных стран.Наиболее древние образцы фресок обнаружены при раскопках Критской цивилизации.На полторы тысячи лет моложе их фрески города Помпеи, в 79 году нашей эрыпогребённой под пеплом вулкана Везувий. Эти фрески вновь увидели свет в нашевремя. Благодаря им наши современники смогли многое узнать о жизни Римскойимперии. Например, на одной из фресок запечатлена работа штукатуров, которые«устраивают особые водоёмы, где мешают известь с песком… а затем… вводят вдействие рабочие команды и заставляют их бить это месиво деревянным пестиком».Такая обработка штукатурки, по свидетельству современников, обеспечивала особуюпрочность получаемых облицовок, по которым затем и выполняли росписи. Вообще,качеству грунта – штукатурки – во фресковой живописи придаётся очень большоезначение, поскольку от него зависит долговечность создаваемых картин. На Русиизвесть, применяемая для фресок, проходила многолетнюю обработку: в течениетрёх-восьми лет её выдерживали в особых ямах, постоянно перелопачивая. Дляполучения штукатурки известь смешивали с гипсом, мелом, мелко точёным кирпичом,рубленным льдом. Грунт обычно держали двухслойным. На хорошо просохший первый,достаточно толстый слой штукатурки непосредственно перед началом работыхудожники наносили тонкий второй слой, по которому выполняли роспись.
Фреска составляет целую эпоху в развитии западноевропейскойживописи. До нашего времени дошли великолепные росписи Джотто, Микеланджело,Рафаэля, Гойи и других прославленных мастеров. К сожалению, немало фресокпогибло. Среди них работы Леонардо да Винчи (1452-1519 гг.). Гениальный художники экспериментатор, он постоянно стремился к усовершенствованию техникиживописи. Однако его попытка писать масляными красками по фресковому грунтуоказалась неудачной: фреска «Тайная вечеря» в трапезной миланского монастыряСанта-Мария деле Грацие начала осыпаться вскоре после её создания. Разрушениевеликого творения Леонардо довершили неумелые реставрации и солдаты Наполеона,устроившие в трапезной конюшню.
О величии фресок итальянского Возрождения можно судить потворениям Рафаэля и Микеланджело. Совсем недавно в личной молельне римских пап– Сикстинской капелле – проведена реставрация колоссальных фресок Микеланджело«Сотворение мира» и «Страшный суд» общей площадью около <st1:metricconverter ProductID=«750 кв. метров» w:st=«on»>750 кв. метров</st1:metricconverter>.Состояние стен капеллы было проверено с помощью самой современной электроннойаппаратуры, а для анализа химического состава использованных художником красокприменены наиболее совершенные физико-химические методы. Реставраторы очистилиповерхность красочного слоя специальным составом и нанесли слой акрилового лакана защищаемую поверхность.
В подобной заботе нуждаются и памятники отечественнойкультуры. Огромного уважения заслуживают усилия художников А.П. Грекова, Н. В.Гусева, А.К. Крылова и других, стремящихся сохранить для потомков дошедшие донашего времени древние фресковыеросписи.
Какими красками писали западноевропейские художникиСредневековья и Возрождения, византийские и русские иконописцы? Оказывается, доXVвеканаиболее распространённой техникой живописи была темпера.
Андрей Рублев и Семён Холмогорец, Мозаччо и Дюрер, Кранах иБрейгель Старший, Тициан и Рафаэль, как и многие их современники, писалитемперными красками, для приготовления которых пигменты растирали на различныхэмульсиях. Готовые темперные краски можно развести водой. Но после их высыханияэта способность растворяться в воде утрачивается. Свойства темперных красокзависят от характера использованных эмульсий. Классическая яичная темперанедостаточно эластична, это приводит к тому, что при изменении условийокружающей среды (температуры, влажности) живописный слой не способенрасширяться и сокращаться вместе с грунтом и основой и неизбежно покрываетсясеточкой тонких трещин (кракелюр). Поэтому в старину для повышения эластичностикрасок применяли различные добавки: итальянские живописцы использовали вино исок фигового дерева, немецкие – спирт и пиво, содержащие растительнуюклейковину, русские изографы брали хлебный квас. Названные добавкиспособствовали также улучшению текучести красок и служили консервантами, тоесть препятствовали развитию процессов гниения.
Технология создания темперного полотна очень сложна.Живопись многослойна, каждый её фрагмент пропитывается много раз, и всякий разнеобходимо ждать полного высыхания красок. На Руси в технике темперы в старинуписали иконы. Икон, относящихся к до-монгольскому периоду, осталось немного –около 30. самая ценная из уцелевших – икона «Апостолы Пётр и Павел» (середина XI века), находившаяся вновгородском соборе Святой Софии.
Русские иконы обычно писали на сосновых, липовых или еловыхдосках. Сухие, выдержанные в течение нескольких лет доски скоблили, шлифовали,делали в центральной части углубление – ковчег. На подготовленную доскунакладывали кусок холста – паволоку, а на неё последовательно наносили додесяти слоёв левкаса (грунта), состоящего из смеси мела, муки и мёда, которыйиграл роль связующего. В других случаях в качестве связующего использовалимездровый или рыбий клей. Первый готовили из обрезков кожи животных, второй изплавательных пузырей осётровых рыб (это сырьё содержит белок с относительнонебольшой молярной массой, что придаёт клею необходимые свойства). Рыбий клейвсегда был дорог. В средние века новгородские купцы вывозили его за границу вчисле самых ценных товаров. Левкас был жидким. Его составляющие растирали тактонко, что после высыхания десяти последовательно нанесённых слоёв получаласьплёнка толщиной около <st1:metricconverter ProductID=«1 мм» w:st=«on»>1 мм</st1:metricconverter>.По левкасу писали красками. Здесь тоже существовал строгий, раз и навсегдаустановленный порядок. Святых изображали в соответствии с канонами иконописныхподлинников. В светской живописи XV-XVIIвв. темпера была вытеснена менее сложной техникой масляной живописи. Однако ссередины XIX столетиятемпера вновь обрела былую популярность. Ею пользуются и современные художники,а частности миниатюристы старинного художественного центра России села Палех аИвановской области. Здешние мастера, продолжая и развивая традиции русскойиконописи, создают великолепные произведения искусства.
Среди важнейших техник живописи масляная – наиболее «молодая». Легенда приписывает её созданиевеликому нидерландскому художнику Яну Ван Эйку (1390-1441 гг.) – придворномуживописцу бургундского герцога ФилиппаДоброго, жившему в г. Бюрге. Однако не все историки отдают приоритет Ван Эйку.Дело в том, что использование красок, стёртых на растительном масле,практиковалось и до него. К тому же в темперной живописи традиционноприменялись некоторые краски, «не терпящие желтка», и поэтому стёртые нальняном или ореховом масле. Таким образом, не ван Эйк первым применил масло.Однако общепризнанно, что ему удалось улучшить технику масляной живописи. Повпечатлениям современников, его картины убедительно передавали иллюзиюнаполненного светом пространства, предметного мира. Благодаря изысканиямвеликого нидерландца растительные масла оказались «материалом, который придавалкраскам для живописи совершенно новые качества и удовлетворил художников вотношении почти неограниченных возможностей передачи действительности».
Для приготовления красок использовали высыхающие масла:маковое, ореховое (из ядер грецких орехов), конопляное, льняное. Из них лучшее,придающее краскам необходимые свойства, — льняное, так как оно содержитнаибольшее количество триглицеридов – ненасыщенных карбоновых кислот. Приконтакте с воздухом все перечисленные масла высыхают: ненасыщенные карбоновыекислоты окисляются и полимеризуются. В результате образуется прочная прозрачнаяплёнка. Линоксин – плёнка, образуемая, льняным маслом, — отличается наибольшейпрочностью и эластичностью.
В первое время все необходимые художественные материалы длямасляной живописи готовили непосредственно под руководством художников. Мастеравладели множеством технологических секретов, которые нередко являлись фамильнымдостоянием. Ещё в XVIIIвеке готовыми красками, продававшимися в лавках, рекомендовали пользоватьсяразве что любителям. В начале XIXстолетия производство красок перешло в руки промышленников. Это было и хорошо иплохо. С одной стороны, художники наконец избавились от нелёгкого и хлопотноготруда по приготовлению необходимых материалов, с другой – массовая продукция(холсты, грунты, краски, связующие) не всегда обеспечивала достаточно высокоекачество живописи.
В XXвеке две знаменитые картины были порезаны ножом. Потом оба полотна удалосьвосстановить (одно из них можно видеть в Третьяковской галерее, другое – вЛондонской национальной галерее). Это картины «Иван Грозный и сын его Иван»И.Е. Репина и «Венера с зеркалом» Д. Веласкеса. При реставрации выяснилось, чтос картины Репина краска осыпалась не только там, где прошёл нож, но и в техместах, где преступник дотронулся до картины рукой, а с картины Веласкесакраска не осыпалась вовсе. Объяснить это можно разным качеством грунтов.Великий испанский художник XIIвека Диего Веласкес, подобно всем старым мастерам, грунтовал холсты сам, посвоим собственным рецептам. Репин – художник другого времени – покупал готовыехолсты у дрезденской фирмы «Цвиллих», которые были покрыты плотным маслянымглянцевым грунтом. Эта фирма выпускала холсты с середины XIX века, имела немалую популярность, иеё продукция пользовалась большим спросом. Вероятно – и это красноречивоподтверждают быстро стареющие и разрушающиеся картины, — при изготовлениихолстов недостаточно долго выдерживались грунты. Современные промышленныепредприятия выпускают материалы весьма высокого качества, и тем не менеехудожники иногда предпочитают собственноручно изготовлять необходимые им дляработы холсты и краски.
Акварель – одиниз самых поэтичных видов живописи. Лирическую, полную светлых и ясных образовлитературную зарисовку или новеллу часто называют акварелью. Можно писать посухой или сырой бумаге сразу, в полную силу цвета. Можно работать вмногослойной технике, постепенно уточняя цветовое состояние, каждую частность.Нельзя или почти нельзя исправить испорченное место: акварель не выноситмалейшей затёртости, замутнённости, неясности. Прозрачность и блеск передаёт ейбумага, которая должна быть белой и чистой. В полной мере акварель утвердиласьв странах Европы в конце XVII– начале XVIII вв.одними из первых её оценили английские живописцы. Особенно прославилсяУ.Тернер. Также в России было немало выдающихся акварелистов: К.П. Брюллов,А.А. Иванов, П.А. Федотов и другие.
Гуашь – впереводе с французского означает «водяная краска». Гуашевые краски обладаютбольшими кроющими возможностями, непрозрачны, хотя и разводятся водой. Втехнике гуаши художники пишут по бумаге, картону, фанере, плотному шёлку.Работы имеют матовую, бархатистую поверхность. Но при использовании гуашивозникают свои трудности – краски после высыхания быстро светлеют. Требуетсянемалый опыт, чтобы предугадать степень изменения плана и цвета.
Пастелью называютцветные карандаши без оправы, изготовленные из красочного порошка. Название«пастель» происходит от итальянского слова «паста» — «тесто». Его получаютпутём смешивания красочного порошка и количество клея придают различную степеньмягкости пастели. Работают в этой технике на бумаге, картоне и холсте. Краскинаносятся штрихами или втираются пальцами и растушёвкой, что позволяетхудожнику добиваться тончайших красочных нюансов и нежнейших переходов тонов,матовой, бархатистой поверхности. При работе пастелью можно легко снимать илиперекрывать целые красочные слои, так как она свободно соскабливается с грунта.Но эта же особенность делает её чрезвычайно восприимчивой к внешнимвоздействиям, поэтому произведения, выполненные пастелью, обычно закрепляютсяспециальным раствором, который приглушает световую переливающуюся поверхность инередко вызывает потемнение. Пастель иногда применяют в комбинации с темперойили гуашью, реже с масляными красками.
Методы исследования произведениймонументальной и станковой живописи.
1 декабря 1863 года заведующим кафедры геологии, физики иэлементарной химии Парижской школы изящных искусств был назначен Луи Пастер.Трудно было найти лучшую кандидатуру. Сфера интересов Пастера была необычайноширокой, увлекался он живописью: в молодости учился с Густавом Курбе.Исследователь произведений искусств, он утверждал, что этим должны заниматьсяне только искусствоведы, но и химики; Пастер понял это одним из первых. Наодной лекции он говорил: «Мы совершенно ничего не знаем о приёмах техникипервых живописцев, писавших маслом…»; «К чему бесконечно спорить о том,применяли ли эти мастера лак в своих картинах, и выяснять, каким был состав ихгрунта? Изучите химически живопись. Это единственно научный метод, посколькуэрудиция тут бессильна».
Между тем художники,не дожидаясь конца теоретических споров, экспериментировали каждый по-своему.Чаще всего, не мудрствуя лукаво, они пытались согласно старинным трактатамсоставить из растительных масел и лаков идеальное связующее, которое помогло бывоссоздать краски старых мастеров. Однако ничего не получалось.
Химики тоже не дремали. В 1850 году вышла работа М.Шевреля«Исследование масел, употребляющихся в живописи». Она заложила основы новогонаправления в органической химии - химиимасел. В 1884 году немецкий химик А.Кейм основал журнал «Технические сообщениядля живописи», а два года спустя – Немецкое общество содействия рациональным методамживописи. В него входили учёные и художники; одним из членов общества былпрофессор Петербургского университета Ф.Ф. Петрушевский.
Но систематические поиски химических методов, которыми можноизучать состав старинных красок, начались в самом конце XIXвека. Так,для определения пигментов стали использовать микрохимические капельные реакции.Пытались определить связующее по его способности растворяться в воде, кислотахи щелочах; белки – по присутствию азота, серы. Вот как, например, можноидентифицировать связующее по способу американского учёного Р. Геттенса. При слабом нагревании образцов сразбавленной азотной кислотой, указывал он, появлялась «типичная маслянаякапля». Обработка холодным 5-процентным раствором едкого натра частичноразрушала красочную плёнку, но не полностью растворяла её. На этом основанииГеттенс делал вывод, что связующим красок было масло. Такие эксперименты,разумеется, неточны и мало достоверны.
Определением связующих заинтересовался и знаменитый химикВильгельм Оствальд. В 1905 году онпредложил новый и неожиданный подход к проблеме: гистологический. Небольшуюкрупинку живописи Оствальд зажимал между кусками пробки и разрезал на микротоме– приборе, на котором гистологи режут ткани для изучения их срезов подмикроскопом. Так же поступил и Оствальд: срезы он помети в каплю воды напредметное стекло и обрабатывал их специфическими красителями (теми же, кстати,что и гистологи; скажем, метилвиолетом – для обнаружения масел, йодэозином — для обнаружения белков). «Теперь могут бытьвыявлены подделки, — писал он, — и записанные картины могут быть отличены отподлинно сохранившихся».
Оствальд оказался прав – метод срезов широко применяется дляизучения живописи и по сей день. Только фрагмент не зажимают между кускамипробки, а пускают в жидкую полиэфирную смолу, которая затвердевает приполимеризации. Блок разрезают, и тонкие срезы окрашивают красителями. Если насрезе появляются устойчивые окраски с беловыми реагентами, это означает, чтоприменялись белковые связующие – белок яйца, казеин молока, желатин. Если срезокрашивается красителями, взаимодействующими с липидами, то связующие – масло.Если же оба реактива окрашивают срез, то, вероятно, мы имеем дело с красками,замешанными на яичном желтке, — в нём есть и липиды и белки.
В живописном слое картины Боттичелли «Мадонна с младенцем исв. Иоанном» (1490-е годы) были обнаружены пять слоёв краски. Окрашивание срезапоказало, что один из нижних слоёв содержал яичный белок, а остальные – масло.Другими словами, художник сначала набрасывал композицию темперой, а продолжал изаканчивал работу масляными красками (искусствоведы же всегда считали, что онработал исключительно маслом).
Этот метод даёт нам возможность отличить белковое связующееот масляного. Но что за белок, что за масло, таким способом не узнать. Тутнужны биохимические исследования.
Изучение химического состава древнейживописи в инфракрасных лучах.
До сих пор точно неизвестно, какими красками писали античныехудожники: пользовались ли они воском или расписывали стены домов в техникефрески – без связующего. Искусствоведы спорят об этом около двухсот лет.Химические исследования помпейской живописи, проведённые в конце XIX – начале XX веков, показали, что в росписи внутреннихпомещений воска нет, но он есть в красках наружных стен. Однако опыт последнегодесятилетия вновь запутал проблему: и во внутренних помещениях были обнаруженыкраски на воске, а также на растительных клеях – растворах камедей. Восковыекраски внешне почти не отличаются от масляных. Но энкаустическая живописьсохраняет цвет, яркость, первоначальную чистоту исполнения в течение несколькихстолетий. Исследования показали, что для неё опасны только механическиеповреждения, так как восковая краска мягкая. Воск – это вещество растительногоили животного происхождения. По химической природе он близок к жирам и восновном состоит из сложных эфиров высших жирных кислот и высших спиртов.
Археологи передали нам фрагменты росписей Iвека до нашейэры из раскопок Пантикапея – города, находившегося на месте современной Керчи.Это были толстые куски штукатурки с красной или жёлтой раскраской. Поверхностьих оказалась ровной и блестящей, но был ли обусловлен этот блеск воском?
Счищенную краску проэкстрагировали хлороформом (пигменты внём не растворялись, в древние времена пользовались минеральными пигментами).Растворённое вещество исследовали и с помощью инфракрасной спектроскопии. Спектр поглощения вещества,если нём отсутствуют существенныепримеси, очень специфичен, его трудно спутать с другим и легко сопоставить сизвестными. Спектр вещества оказался знакомым: это был спектр пчелиного воска.Для сравнения проэкстрагировали кусочек краски византийской иконы VI века «Сергий и Вакх»,написанной восковыми красками. Спектры оказались очень похожими. Единственноеотличие между ними – присутствие в спектре византийской живописи дополнительнойполосы поглощения, которая характерна для солей жирных кислот. Это значит, чтодля иконы применяли воск, проваренный с морской водой и содой (так называемыйпунический), а для стенной живописи – просто воск.
Исследовали также росписи, открытые в развалинахсреднеазиатских городов. Внешне эта живопись выдержана в традициях буддийскогоискусства, но о том, как работали художники, ничего не было известно. Началобиохимическому изучению живописи положил ещё в 1927 году профессор И.И.Андреев. Он предположил, что средневековые росписи в Хара-Хото – заброшенномгороде, открытом в начале века в пустыне Гоби,- написаны красками, замешаннымина яичном желтке. Андреев для доказательства привёл опыт с сывороткой кроликов.Специфические антитела, вырабатывающиеся в организме кроликов, реагировали наприсутствие в красках желтка, раствор сильно мутнел (реакция преципитации).
Уже в наши дни американские исследователи М. Джонсон иЭ.Паккард воспользовались реакцией преципитации с более совершеннымисыворотками, способными выявлять только определённые виды веществ, то естьуточняющими результаты исследований.
Металлы – материал для создания шедевровмирового искусства.
Металлы – химические элементы, образующие в свободномсостоянии простые вещества с металлической химической связью. В основеструктуры металлов лежит кристаллическая решётка из положительно заряженныхионов, погруженных в плотный «газ» подвижных электронов. Такое строение иобусловливает важнейшие физические свойства металлов: пластичность,электропроводность, теплопроводность, металлический блеск, прочность, которыешироко используются как в народном хозяйстве, так и в искусстве.
О меди и бронзе.
Смена эпох разныхнародов, в разных точках земного шара происходила неравномерно, и иххронологические рамки могут быть названы лишь приблизительно.
Историками установлено, что в период Древнего царства вЕгипте (2960-2270 гг. до н.э.), в эпоху постройки египетских пирамид,ремесленники применяли исключительно медныеинструменты (каменный инвентарь делали из гранита и долерита). Некоторые изних отличались поразительной твердостью. Это позволило египтологампредположить, что уже в 3-м тысячелетии до н.э. египтяне владели секретамизакаливания меди.
Учёным удалось расшифровать письменные источники периодаНового царства (1550-1090 гг. до н.э.), из которых стало известно, что наважнейшей государственной службе Древнего Египта – строительство гробниц фараонв Дель эль Медине – среди представителей разных профессий были и медники.
В то время не знали о совмещении профессий, напримерживописец никогда не выполнял работы скульптора. Труд художников оценивался также, как труд любого ремесленника: эстетическая ценность созданного при этом врасчёт не принималась. Профессиональное разделение осуществлялось не по уровнюмастерства или творчества, а по материалу и характеру применяемых инструментов.Труд медника в период Древнего царства был весьма уважаем, хотя и менеепрестижен, чем работа мастера по золоту или дереву. Однако с течением времени ктяжёлой профессии медника и её обладателям стали относиться с меньшим почтением, а в периодНового царства – и с откровенным презрением. Конкретным проявлением изменившегосяположения стал перевод медников в низшее сословие, называемое «люди».Исключённые из ранга мастеров медники подчинялись «хранителям». Роль последнихсостояла в следующем: для каждого изготовленного медного орудия делалась гиря,точно соответствовавшая его массе. Инструменты со специальным «доверенным»отправлялись на строительство, а гиря сохранялась в особой кладовой. Когдаорудие изнашивалось, с помощью гири определяли процент потери меди.Хранитель выдавал меднику недостающееколичество металла, и инструмент шёл в перековку. Современным историкамизвестна даже норма выработки медника: в течение рабочего дня он должен былобработать <st1:metricconverter ProductID=«3 кг» w:st=«on»>3 кг</st1:metricconverter>металла. Орудия, прошедшие многократную перековку и отслужившие несколькосроков, хранились в строжайшем порядке с пометкой «старая медь».
Таким образом, во 2-м тысячелетии до н.э. медники занималисьв основном
www.ronl.ru
Химическая картина мира
Химия – наука о превращениях веществ, сопровождающихся изменением их состава и строения.
Явления, при которых из одних веществ образуются другие, называются химическими. Естественно, что, с одной стороны, в этих явлениях можно обнаружить чисто физические изменения, а, с другой стороны, химические явления всегда присутствуют во всех биологических процессах. Таким образом, очевидна связь химии с физикой и биологией.
Эта связь, по-видимому, была одной из причин того, почему химия долго не могла стать самостоятельной наукой. Хотя уже Аристотель разделял вещества на простые и сложные, чистые и смешанные и пытался объяснить возможность одних превращений и невозможность других, химические явления в целом он считал качественными изменениями и потому относил к одному из родов движения. Химия Аристотеля была частью его физики – знания о природе (  ).
).
Другая причина несамостоятельности античной химии связана с теоретичностью, созерцательностью всей древнегреческой науки в целом. В вещах и явлениях искали неизменное – идею. Теория химических явлений приводила к идее элемента ( 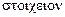 ) как некоего начала природы или к идее атома как неделимой частицы вещества. Согласно атомистической концепции, особенности форм атомов во множестве их сочетаний обуславливают разнообразие качеств тел макромира.
) как некоего начала природы или к идее атома как неделимой частицы вещества. Согласно атомистической концепции, особенности форм атомов во множестве их сочетаний обуславливают разнообразие качеств тел макромира.
Эмпирический опыт относился в Древней Греции к области искусств и ремесел. Он включал также и практические знания о химических процессах: выплавке металлов из руд, крашении тканей, выделке кожи.
Вероятно, из этих древних ремесел, известных еще в Египте и Вавилоне, возникло «тайное» герметическое искусство Средневековья – алхимия, наиболее распространенное в Европе в IX-XVI веках.
Зародившись в Египте в III-IV веках, это направление практической химии было связано с магией и астрологией. Целью ее было разработать способы и средства превращения менее благородных веществ в более благородные, чтобы достичь реального совершенства, как материального, так и духовного. В ходе поисков универсальных средств таких превращений арабские и европейские алхимики получили много новых и ценных продуктов, а также усовершенствовали лабораторную технику.
Если считать, что химия становится наукой в XVII-XVIII веках, то можно выделить три периода формирования современной химической картины мира.
1. Период зарождения научной химии (XVII – конец XVIII в.; Парацельс, Бойль, Кавендиш, Шталь, Лавуазье, Ломоносов). Характеризуется тем, что химия выделяется из естествознания в качестве самостоятельной науки. Ее цели определяются развитием промышленности в Новое время. Однако, теории этого периода, как правило, используют либо античные, либо алхимические представления о химических явлениях. Завершился период открытием закона сохранения массы при химических реакциях.
Например, ятрохимия Парацельса (XVI в.) была посвящена приготовлению лекарств и лечению болезней. Парацельс объяснял причины болезней нарушением химических процессов в организме. Как и алхимики, он сводил разнообразие веществ к нескольким элементам – носителям основных свойств материи. Следовательно, восстановление их нормального соотношения приемом лекарств излечивает болезнь.
Теория флогистона Шталя (XVII-XVIII вв.) обобщала множество химических реакций окисления, связанных с горением. Шталь предположил существование во всех веществах элемента «флогистон» – начала горючести.
Тогда реакция горения выглядит так: горючее тело → остаток + флогистон; возможен и обратный процесс: если остаток насытить флогистоном, т.е. смешать, например, с углем, то снова можно получить металл.
2. Период открытия основных законов химии (1800-1860 гг.; Дальтон, Авогадро, Берцелиус). Итогом периода стала атомно-молекулярная теория:
а) все вещества состоят из молекул, которые находятся в непрерывном хаотическом движении;
б) все молекулы состоят из атомов;
в) атомы представляют собой мельчайшие, далее неделимые составные части молекул.
3. Современный период (начался в 1860 гг.; Бутлеров, Менделеев, Аррениус, Кекуле, Семенов). Характеризуется выделением разделов химии в качестве самостоятельных наук, а также развитием смежных дисциплин, например, биохимии. В этот период были предложены периодическая система элементов, теории валентности, ароматических соединений, электрохимической диссоциации, стереохимия, электронная теория материи.
Современная химическая картина мира выглядит так:
1. Вещества в газообразном состоянии состоят из молекул. В твердом и жидком состоянии из молекул состоят только вещества с молекулярной кристаллической решеткой (СО2, h3O). Большинство твердых тел имеет структуру либо атомную, либо ионную и существует в виде макроскопических тел (NaCl, CaO, S).
2. Химический элемент – определенный вид атомов с одинаковым зарядом ядра. Химические свойства элемента определяются строением его атома.
3. Простые вещества образованы из атомов одного элемента (N2, Fe). Сложные вещества или химические соединения образованы атомами разных элементов (CuO, h3O).
4. Химические явления или реакции – это процессы, в которых одни вещества превращаются в другие по строению и свойствам без изменения состава ядер атомов.
5. Масса веществ, вступающих в реакцию, равна массе веществ, образующихся в результате реакции (закон сохранения массы).
6. Всякое чистое вещество независимо от способа получения всегда имеет постоянный качественный и количественный состав (закон постоянства состава).
Основная задача химии – получение веществ с заранее заданными свойствами и выявление способов управления свойствами вещества.
studopedya.ru
Презентация Химия и искусство

Химия в моей профессии
Колледж декоративно-прикладного искусства им.Карла Фаберже.
Маковская З. Г

Химия и искусство
Химия и искусство имеют внутреннюю общность, которая коренится в их творческой природе.
Марселен Бертло
С помощью усовершенствования технологий мы наблюдаем различные изобретения человека в плане искусства.
Многие из шедевров дошли до нас из глубины веков и радуют до сих пор, а некоторые были утрачены из-за непрочности материалов. Чтобы добиться наилучшего качества своих красок и долговечности полотен, художнику зачастую нужно быть не только изографом, но и химиком.

Выбор ткани и подготовка её к работе
Ручную роспись можно делать на тканях с разным волокнистым составом: хлопчатобумажных, льняных, вискозных, ацетатных, триацетатных, капроновых, шерстяных и на натуральных шелках.
Наилучшими для росписи являются ткани из натурального шелка. Они тонкие, не имеют на поверхности пушистости, краски на них хорошо растекаются и равномерно покрывают плоскость рисунка без ореолов, пятен, затеканий. Из этих тканей в росписи применяют: туаль, полотно, крепдешин, креп-жоржет, креп-шифон.

Холодный батик
Холодный батик основан на том, что при этом способе росписи тканей все формы рисунка, как правило, имеют замкнутую контурную обводку , что придает своеобразный характер рисунку. Правильно приготовленный резерв имеет хорошие текучесть и пластичность, пропитываемость ткани. В его состав входят: резиновый клей, бензин, воск, парафин, вазелин и канифоль.

Вспомогательные материалы:
Парафин — воскоподобное вещество, смесь предельных углеводородов (алканов) состава от С18Н38 до С35Н72.
Парафины представляют собой смесь твёрдых углеводородов метанового ряда преимущественно нормального строения с 18-35 атомами углерода в молекуле и температурой плавления 45-65 °C.
Парафин — вещество белого цвета кристаллического строения с молекулярной массой 300—450, в расплавленном состоянии обладает малой вязкостью.
Бензи́н — горючая смесь лёгких углеводородов с температурой кипения от 30 до 200 °C. Бензин получают путем разгонки и отбора фракций нефти, выкипающих в определенных температурных пределах

Свободная роспись ткани
Свободная роспись выполняется без использования резервных смесей.
Известно несколько способов свободной росписи ткани: красками с применением солевого раствора; красками с загусткой из резерва; печатными красками; по тканям, аппретированным загустками; масляными красками. Все вышеназванные способы свободной росписи требуют запарки, кроме росписи масляными красками.

Узелковый батик
Узелковое крашение применяют для получения одно- или многоцветных эффектов на материалах.
Суть состоит в том, что перед крашением ткань по предварительно продуманной схеме складывают определенным способом и перевязывают прочными нитками или тонкими шнурами. После этого ткань красят по технологии гладкого крашения.

Краски для ручной росписи тканей
В процессе изготовления красок для холодного и горячего батика применяют красители, которые хорошо растворяются в воде, спирте, имеют хорошие покрывные свойства в растворах комнатной температуры, дают широкую гамму чистых и ярких цветов.
Этим требованиям отвечают активные, прямые, кислотные, хромовые, основные и дисперсные красители.
![АКТИВНЫЕ КРАСИТЕЛИ Общая формула активных красителей: (Р)n - Кр - А где Кр - хромофорная часть молекулы; А - активный центр; Р - группы, придающие красителю растворимость (OH, SO3H, SO3Na). ПРЯМЫЕ КРАСИТЕЛИ Производятся прямые красители в виде Na-солей диссоциирующих в воде с образованием окрашенных анионо, где Кр-остаток молекулы красителя. КИСЛОТНЫЕ КРАСИТЕЛИ. С одержат в молекуле группы SO3H, реже СООН и поэтому хорошо раств. в воде. Производятся в виде Na-солей, диссоциирующих в воде с образованием окрашенных анионов: KpSO3NaDKpSO3+Na+, где Кр остаток молекулы красителя. ХРОМОВЫЕ (КИСЛОТНО-ПРОТРАВНЫЕ) КРАСИТЕЛИ Na2Cr2O7·2h3O или К2Сr2О7 ОСНОВНЫЕ КРАСИТЕЛИ , водорастворимые соли орг. оснований, диссоциирующие в воде с образованием окрашенного катиона и бесцв. аниона [Сl-, НСОО-, СН3СОО- и др.]](/800/600/http/arhivurokov.ru//multiurok/f/9/8/f98ed8e0389e4d8c4612a8399c72660c054b3a82/img8.jpg)
АКТИВНЫЕ КРАСИТЕЛИ Общая формула активных красителей:
(Р)n - Кр - А
где Кр - хромофорная часть молекулы;
А - активный центр;
Р - группы, придающие красителю растворимость (OH, SO3H, SO3Na).
ПРЯМЫЕ КРАСИТЕЛИ Производятся прямые красители в виде Na-солей диссоциирующих в воде с образованием окрашенных анионо, где Кр-остаток молекулы красителя.
КИСЛОТНЫЕ КРАСИТЕЛИ. С одержат в молекуле группы SO3H, реже СООН и поэтому хорошо раств. в воде. Производятся в виде Na-солей, диссоциирующих в воде с образованием окрашенных анионов: KpSO3NaDKpSO3+Na+, где Кр остаток молекулы красителя.
ХРОМОВЫЕ (КИСЛОТНО-ПРОТРАВНЫЕ) КРАСИТЕЛИ Na2Cr2O7·2h3O или К2Сr2О7
ОСНОВНЫЕ КРАСИТЕЛИ , водорастворимые соли орг. оснований, диссоциирующие в воде с образованием окрашенного катиона и бесцв. аниона [Сl-, НСОО-, СН3СОО- и др.]

Натуральные красители
До середины прошлого столетия краски, которыми окрашивали ткани в Европе и в других частях света, были растительного происхождения. Они получались из цветов, плодов, листьев, из древесины, коры, болезненных наростов на растениях - таких, например, как чернильные орешки - нарост на листьях некоторых видов дуба.

Горячий батик
Горячий батик — одна из разновидностей батика. Узор создается с помощью расплавленного воска или других подобных веществ. Окрасив ткань и сняв воск, мы получим белый или разноцветный рисунок на цветном фоне.
Во́ски — распространённые в растительном и животном мире сложные эфиры высших жирных кислот и высших высокомолекулярных спиртов. Очень устойчивы, нерастворимы в воде.
По происхождению воски можно разделить на животные, растительные и ископаемый воск (состоит главным образом из предельных углеводородов).

Химические вещества и материалы в живописи
Краска состоит из пигмента и связующего вещества (масло, клей и др.). Пигменты – это цветные порошки, нерастворимые в органических растворителях (лаках, маслах), а также в воде. Красители – другие красящие вещества – образуют с водой растворы. Наиболее прочны краски, приготовленные на природном минеральном сырье, менее прочны – органические краски. Минеральные краски бывают натуральные (охры, сиены, умбры, азурит, малахит, горная киноварь и др.) и искусственные – получаемые путем химического синтеза нескольких веществ, прокаливания при высоких температурах.

Основные виды красок:
Эмульсионные краски бывают акриловые, водоэмульсионные, латексные, поливинилацетатные, водно-дисперсионные. Они применяются для окраски бетонных, загрунтованных металлических, оштукатуренных и деревянных поверхностей и непригодны для нанесения на клеевые краски и лакированные поверхности .
Алкидные К этому виду красок относятся масляные краски, которые производятся на основе олифы, а также краски на основе лака – эмалевые. Они водо- и светоустойчивы, нетоксичны.
Силикатные краски производятся они на основе жидкого стекла и поэтому относятся к разряду минеральных.
Клеевые Производство клеевых красок основано на водных растворах органических полимеров: крахмала, эфира целлюлозы, казеина, поливинилового спирта. По свои свойствам они близки к эмульсионным, но в отличие от них, менее устойчивы к влаге.

Заключение:
Батик — batik — индонезийское слово. Часть слова — tik — на всех индонезийских языках означает «точка» или «капля»; -ба — хлопчатобумажная ткань. Ambatik — рисовать, покрывать каплями, штриховать.
Главным в батике, как и в любом виде живописи, является сочетание нескольких условий: оригинальная идея, мастерство художника и качественные материалы, только в этом случае получаются достойные восхищения работы. Здесь и нужна химия, которая позволяет не только получать такие материалы, но и долгое время сохранять свое качество.

Причины такой популярности батика :
Во-первых, доступность материалов, необходимых для создания произведений из батика;
Во-вторых, возможность использования батика в самых различных прикладных областях художественного оформления, интерьера, дизайна и т.д.;
В-третьих, батик влечет своей необычайной простотой, легкостью и прозрачностью;
В-четвертых, искусством батика можно заниматься в любом возрасте, в любой точке мира.

Работы студентов
Рис.1 Узелковый батик, ткань: крепдешин
Рис.2 Холодный батик, название: «Настроение», ткань: атлас
Рис.3 Холодный батик, название: «Маки», ткань: крепдешин

Рис.4 Холодный батик, название: «Лесная фея», ткань: фуляр
Рис.5 Холодный батик, название: «Лесная дива»,ткань: крепдешин
Рис.6 Холодный батик, название: «Дома», ткань: эксельсиор
multiurok.ru
Весёлые картинки - химия, прочее
Журнал по технике безопасности.
«Весёлые картинки».
Выполнили учащиеся 8класа
Садыкова Альбина и Барило Данил .
Учитель : Пуклакова Ольга Викторовна.
МБОУ Александровская СОШ .2015г
В кабинете химии ничего нельзя пробовать на вкус!

2. Не нюхай незнакомые вещества.
Неправильно!!!

а вот так правильно!!!

3.Будь аккуратен с реактивами!

4. Всегда помните!!!


5. При выполнении работы будь внимательным !

6. Используй только чистую посуду!

И всё будет хорошо!

kopilkaurokov.ru











